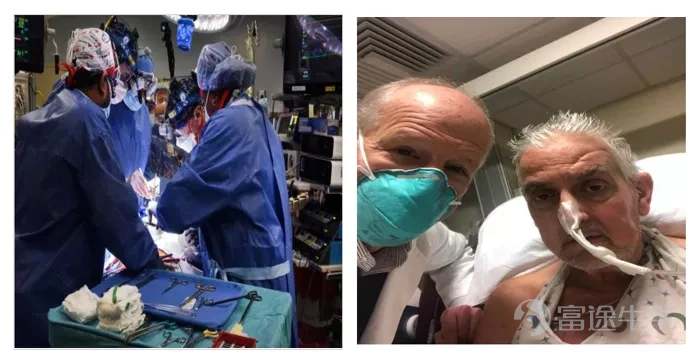
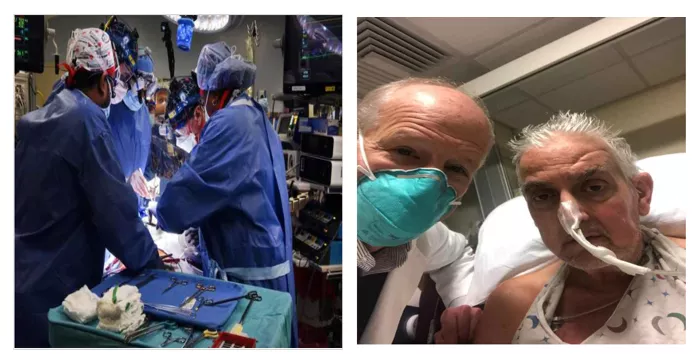
57歲的大衞·貝內特患有晚期心臟病,生命岌岌可危。在審查了他的醫療記錄後,貝內特被認為沒有資格進行傳統的心臟移植或人工心臟泵。豬心是“目前唯一可用的選擇”。
“要麼死,要麼做移植手術。我想活下去。我知道這是在黑暗中的一槍,但這是我最後的選擇,”貝內特在手術前説。
為了推進實驗性手術,馬里蘭大學通過其富有同情心的使用計劃在新年前夜獲得了FDA的緊急授權。
大衞·貝內特是幸運的!馬里蘭大學醫學院的醫生們,歷經近八小時,首次成功的將一顆經過基因編輯的豬心臟移植到大衞·貝內特體內。手術3天后,大衞·貝內特的身體狀況仍然良好,沒有發生明顯的器官排斥反應(圖1)。
這是全球首例人類接受豬心臟移植的手術,這顯然是一項開創性的手術,如果被證明成功,將為數以萬計的器官衰竭的患者帶來了希望。
豬:人類異種移植的理想器官來源
器官再生工程的一個重要選擇是使用其他物種的活體捐贈作為來源。這種方法的優勢是巨大的,自然活着的器官是完全功能性的,但跨物種的免疫反應也帶來了挑戰。克服這一限制必須進行基因工程操作。長期以來人們所知的對動物器官的超急性免疫反應在很大程度上是通過敲除編碼合成細胞表面碳水化合物異種抗原的基因來消除的,其中最重要的基因是GGTG1,它編碼α-1,3-半乳糖苷酶。另外兩個基因(CMAH和B4GALNT2,它們編碼產生N-羥基神經氨酸的蛋白質)和SD(A)異種抗原也已經在基因敲除模型中進行了研究可以減少交叉反應。與異種移植相關的其他挑戰包括與提供器官的動物物種相關的人畜共患病的風險,以及患者本身對接受動物來源的器官的不情願。
豬通常被認為是人類異種移植的理想器官來源。首先,豬和人體器官在大小和形狀上相似,很容易獲得,近交系和遠交系都已用於臨牀前研究。此外,豬可以通過體細胞核移植技術進行克隆,它們的基因組現在可以很容易地通過核酸酶(如鋅指核酸酶,轉錄激活物樣效應核酸酶(TALENS),CRISPR-Cas9)來編輯。最後,由於豬與人類的親緣關係比非人類靈長類動物更遠,與非人類靈長類動物相比,它們通過移植器官傳播病原體的可能性要小得多。
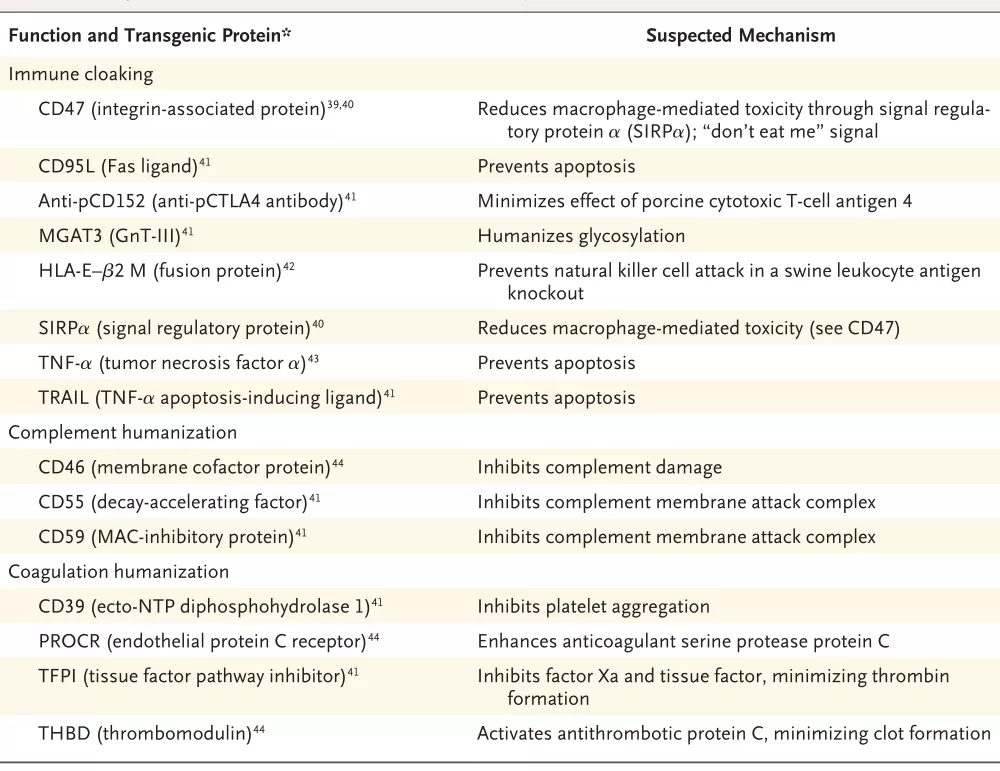
全器官異種移植是在20世紀初進行的,關於它們的消息則是喜憂參半。現在人們認識到由於對糖基化蛋白(如半乳糖-α-1,3-半乳糖)的超急性排斥反應,大多數器官移植很快就失敗了。據報道,通過基因工程敲除負責初級糖基化活動的GGTG1基因的供體豬,能夠極大地減少超急性排斥反應。然而,當這種組織被移植到非人類靈長類動物身上時,它仍然在幾周內被排斥。後續研究人員開展了一系列的研究,以確定主要編碼CD(分化簇)膜蛋白家族的人類基因(圖2),其可表達為轉基因蛋白、融合蛋白或者甚至針對豬蛋白的抗體,以進一步減輕人類抗豬免疫反應。在過去的十年裏,已經對幾種這樣的基因進行了測試,對它們編碼的蛋白主要分為三類:免疫隱蔽,即特定的轉基因蛋白乾擾NK或T細胞的殺傷,以及補體人源化和凝血人源化,即使用人類補體或人類凝血途徑來代替或補充豬的相應途徑。這些干預措施大大促進了異種移植到非人類靈長類動物的成功的可能性,器官排斥反應得到實質性改善。
異種移植的革命性進展及未來
在過去的幾年中,異種移植有兩個引人注目的進展。第一個涉及豬內源性逆轉錄病毒序列(PERV)向轉化的人類組織培養細胞傳播的安全問題。為了徹底消除這種風險,CRISPR-Cas9技術最近被用於消除PK15豬腎臟細胞和成纖維細胞中豬基因組中存在的所有62個PERV拷貝。第二組具有革命進展是產生了器官特異的物種間嵌合體(有時被稱為“外生”),這為在嵌合動物中產生含有完全人類細胞的器官的成功可能性打開了大門(圖3)。

巨大的進步可能使“傳統”異種移植不僅可行,而且實用。對所謂的三基因敲除豬(即GGTA1、CMAH和B4GALNT2基因敲除)進行了研究,這些豬缺乏豬細胞表面的碳水化合物異種抗原,而這些抗原通常被正常的人血清和外周血單核細胞識別。據報道,這種三基因敲除的豬是健康的,體外研究表明,相當大比例的人類羣體對來自這些動物的腎微血管上皮細胞缺乏抗體反應性。此外,在一些患者的樣本中觀察到的交叉反應的程度與在一些人類同種異體移植受者中觀察到的交叉反應的程度相似,這表明對於這類患者,來自這類動物的異種移植排斥反應也許是可以通過使用現有的免疫抑制方案來控制的。對三基因敲除細胞保持免疫反應的人類細胞亞羣似乎識別豬白細胞抗原(SLA)I類(相當於豬的MHCI類)。在隨後的一項研究中,研究者評估了豬SLA基因缺失對移植等待名單上患者血清免疫反應性分析的影響,結果表明,這種SLA缺失可能會增加受益患者的比例。
在人體內移植後,將豬器官的免疫損傷降至最低的第二種方法是補體成分和途徑的工程化。減輕這種損害的一種方法是,通過表達一種或多種下調人類補體活性的人類轉基因蛋白,使豬表面抗原人性化,然後將它們“掩蓋”,使其不被人類免疫系統識別。由於人類補體調節蛋白與人類補體途徑共同進化,人類蛋白有望比豬蛋白更有效地下調補體的作用。這些蛋白包括CD55(補體衰變加速因子)、CD59(膜攻擊複合物抑制蛋白)和CD46(補體調節蛋白)。編碼腫瘤壞死因子α的基因也被認為在控制豬移植的急性血管排斥中起着重要作用,而CD47信號蛋白--它發出“不要吃我”的信息--對促進豬組織的接受性也特別有益。
Hozain等人最近報告了移植領域的另一項跨物種創新,即通過將人肺與豬的循環系統連接起來,使最初被認為過於“受損”而不適合移植的人肺恢復活力。這種體外交叉循環使原本受損的肺恢復到足夠健康的狀態,有可能適合肺移植。這種策略可以大大增加人類肺的可用性。
小編小結
器官移植是再生醫學中最完整的選擇,它為完全的物理和生物修復提供了一種自體、異體或潛在的異種替代。免疫和基因組工程(或編輯)的進展為加速組織和器官異種移植新療法奠定了基礎。在過去的幾年裏,異種移植取得了突破性和革命性的進展。我們期待大衞·貝內特能夠獲得重生,也期待數以萬計的像大衞·貝內特一樣的器官衰竭患者能夠早日擺脱疾病的折磨。
來源:生物製藥小編
風險及免責聲明:以上內容僅代表作者個人觀點,不代表富途任何立場,亦不構成任何投資建議,富途對此不作任何保證與承諾。更多信息
評論
發表評論
1